Участие в соседней группе - Neighbouring group participation
Участие в соседней группе (NGP) (также известный как анхимерная помощь) в органическая химия был определен ИЮПАК как взаимодействие реакционного центра с одинокая пара электронов в атоме или электронов, присутствующих в сигма-облигация или же пи бонд содержится в родительской молекуле, но не сопряженный с реакционным центром.[1][1][2][3] Когда NGP работает, это нормально для скорость реакции быть увеличенным. Также возможно стереохимия реакции быть ненормальной (или неожиданной) по сравнению с нормальный реакция. Хотя соседние группы могут влиять на многие реакции в органической химии (например реакция диен такой как 1,3-циклогексадиен с малеиновый ангидрид обычно дает эндо-изомер из-за вторичного эффекта {перекрытия π орбиталей карбонильной группы с переходным состоянием в Дильс-Альдер реакция}) эта страница ограничена эффектами соседней группы, видимыми с карбокатионы и SN2 реакции.
NGP по неподеленным парам гетероатомов
Классический пример NGP - реакция сера или же азотный иприт с нуклеофил скорость реакции для серного иприта и нуклеофила намного выше, чем для первичного алкил хлористый без гетероатом.

Ph-S-CH2-CH2-Cl реагирует с водой в 600 раз быстрее, чем CH3-CH2-CH2-Cl
NGP алкеном
Π-орбитали алкен может стабилизировать переходное состояние помогая делокализовать положительный заряд карбокатион. Например, ненасыщенный тозилат отреагирует быстрее (1011 раз быстрее для водного сольволиза) с нуклеофилом, чем с насыщенным тозилатом.
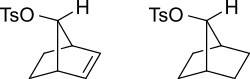
Карбокатионный промежуточный продукт будет стабилизирован резонанс где положительный заряд распределен по нескольким атомам. На схеме ниже это показано.
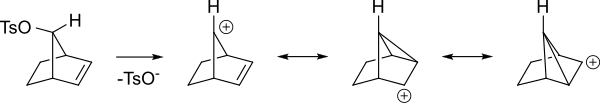
Вот другой взгляд на те же промежуточные звенья.

Даже если алкен находится дальше от реакционного центра, алкен все равно может действовать таким образом. Например, в следующем алкил бензолсульфонат алкена способен делокализовать карбокатион.
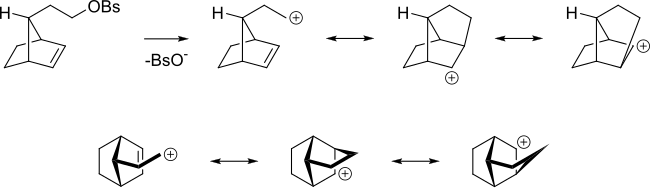
Также увеличение скорости SN2 реакция из аллил бромид с нуклеофилом по сравнению с реакцией н-пропилбромида, потому что орбитали связи π перекрываются с таковыми из переходное состояние. В аллильной системе алкеновые орбитали перекрываются с орбиталями SN2 переходное состояние.
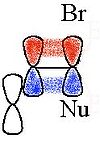
NGP циклопропаном, циклобутаном или гомоаллильной группой
Если циклопропилметилхлорид реагирует с этиловый спирт и воды затем смесь 48% циклопропилметил алкоголь, 47% циклобутанол и 5% гомоаллил получается спирт (бут-3-енол). Это связано с тем, что карбокатионный промежуточный продукт делокализован на многих различных атомах углерода через обратимое отверстие в кольце.

NGP по ароматическому кольцу
В случае бензил галогенида реакционная способность выше, потому что SN2 переходное состояние имеет такой же эффект перекрытия, что и в аллильной системе.

An ароматный кольцо может помочь в формировании карбокатионный промежуточный называется ион фенония путем делокализации положительного заряда.
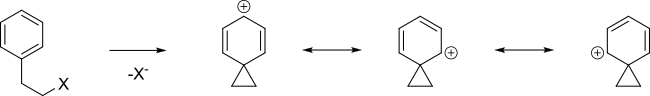
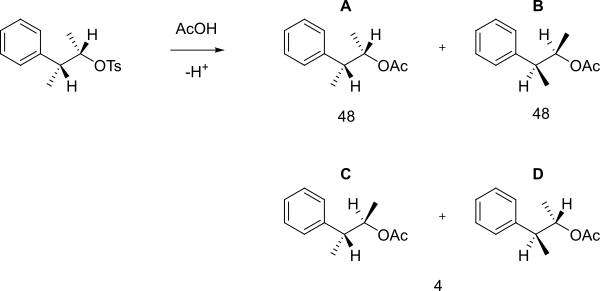
Когда следующие тозилат реагирует с уксусная кислота в сольволиз тогда, а не просто SN2 реакция с образованием B была получена смесь A, B (которые являются энантиомерами) и C + D 48: 48: 4 [2] [3].
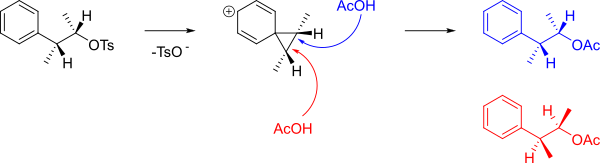
Механизм, образующий A и B, показан ниже.
NGP алифатическими связями C-C или C-H
Алифатические связи C-C или C-H могут привести к делокализации заряда, если эти связи близки и антиперипланарны по отношению к уходящей группе. Соответствующие промежуточные продукты относятся к неклассические ионы, с 2-норборнил система как наиболее известный случай.
внешняя ссылка
Рекомендации
- ^ de Rooij, J. F .; Wille-Hazeleger, G .; Burgers, P.M .; ван Бум, Дж. Х. (1979). «Участие соседней группы в разблокировке фосфотриэфиров нуклеиновых кислот». Исследования нуклеиновых кислот. 6 (6): 2237–2259. Дои:10.1093 / nar / 6.6.2237. ЧВК 327848. PMID 461188.
- ^ Stalford, Susanne A .; Килнер, Колин А .; Лич, Эндрю Дж .; Тернбулл, В. Брюс (07.12.2009). «Участие соседней группы против добавления к ионам оксакарбения: исследования синтеза микобактериальных олигосахаридов». Органическая и биомолекулярная химия. Королевское химическое общество. 7 (23): 4842–4852. Дои:10.1039 / B914417J. PMID 19907773.
- ^ Боуден, Кит (1993-01-01). Бетелл, Д. (ред.). «Участие соседних групп карбонильными группами в гидролизе сложного эфира». Академическая пресса, ScienceDirect. стр. 171–206. Получено 2019-12-17.
- ^ Продвинутая органическая химия, стр. 314, Джерри Марч (4-е изд.), Wiley-Interscience.
- ^ Исследования в Стереохимия. I. Стереоспецифический Перестановка Вагнера-Меервейна из Изомеры 3-фенил-2-бутанола Дональд Дж. Крам Варенье. Chem. Soc.; 1949; 71(12); 3863-3870. Абстрактный
- ^ Исследования по стереохимии. V. Ионные пары сульфоната фенония как промежуточные соединения во внутримолекулярных перегруппировках и реакциях сольволиза, происходящих в системе 3-фенил-2-бутанола Дональд Дж. Крам Варенье. Chem. Soc.; 1952; 74(9); 2129-2137 Абстрактный.
